Cập nhật lần cuối vào 06/04/2023
Buprenorphine là hoạt chất đang được sử dụng ngày càng rộng rãi trong các phác đồ điều trị làm giảm cơn đau liên tục và nghiêm trọng (chẳng hạn như do viêm khớp, đau lưng mãn tính). và hỗ trợ cai nghiện các chất dạng thuốc phiện.
Các công ty dược phẩm không ngừng nghiên cứu phát triển các dạng bào chế cho hoạt chất Buprenorphine như:
Norspan® Miếng dán giải phóng thuốc qua da (Transdermal Patch) chứa Buprenorphine nhiều hàm lượng 5/10/20/40mg, được thiết kế giải phóng thuốc trong vòng 3-7 ngày.



Viên nén ngậm dưới lưỡi (siblingual tablets): chứa 2,16 mg Buprenorphine hydrochloride tương đương 2mg Buprenorphine, cùng một số tá dược vừa đủ 1 viên
Thuốc tiêm: chứa 300 microgram Buprenorphine dạng muối hydrochloride trong 1ml dùng tiêm bắp hoặc tiêm tĩnh mạch
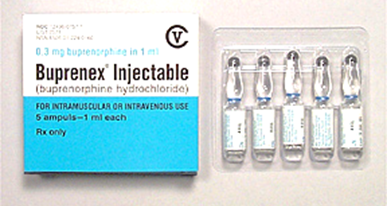
Tuy nhiên, các dạng bào chế từ Buprenorphine dạng ngậm dưới lưỡi sang tiêm dẫn đến một số biến chứng cụ thể như kích ứng da, áp xe chỗ tiêm, viêm nội tâm mạc. Hơn nữa, hình thức điều trị hiện tại đòi hỏi phải uống hàng ngày, gây khó khăn, bất tiện.
Vì tất cả những lý do này, các công thức mới của buprenorphine phóng thích kéo dài (XR-BUP) như Buvidal ® (Camurus ® , Thụy Điển) và Sublocade ® (Indivior ® , Hoa Kỳ) đã được phát triển và thương mại hóa, cung cấp phạm vi điều trị trong một tuần, một tháng hoặc sáu tháng cho các đối tượng cai nghiện opioid.
Bước đột phá nghiên cứu với sự ra đời của que cấy dưới da Probuphine với nhãn hiệu Sixmo ® , đã được phê duyệt ở Hoa Kỳ và Châu Âu. Probuphine là thiết bị cấy dưới da duy nhất được thiết kế để cung cấp buprenorphine liên tục trong sáu tháng sau khi cấy.

1. Dạng bào chế
Probuphine được phát triển bằng cách sử dụng ProNeura™, hệ thống phân phối thuốc liên tục do Titan phát triển, bao gồm một mô cấy nhỏ, rắn được làm từ hỗn hợp ethylene-vinyl axetat và dược chất. Mỗi que cấy chứa buprenorphine hydrochloride tương đương với 74,2mg buprenorphine.
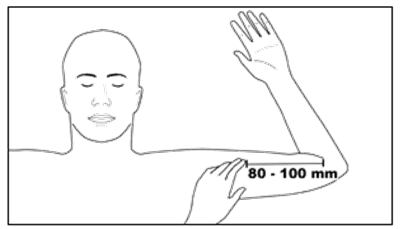
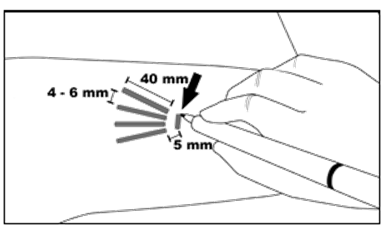
Cấu trúc thu được là một chất nền rắn màu trắng đến vàng nhạt, que cấy hình que, dài 26,5mm và đường kính 2,4mm, được đặt dưới da, thường là ở cánh tay trên trong quy trình tại phòng khám ngoại trú và được lấy ra theo cách tương tự vào cuối giai đoạn điều trị. IXMO được đóng gói trong một hộp gồm 4 bộ phận cấy ghép.
Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã phê duyệt Probuphine vào tháng 5 năm 2016 và đây là thiết bị cấy ghép buprenorphine đầu tiên và duy nhất có sẵn để điều trị duy trì chứng nghiện chất dạng thuốc phiện ở những bệnh nhân đủ điều kiện.
2. Cơ chế tác động
Buprenorphine là opioid có tác dụng dài, cạnh tranh tại thụ thể Muy của hệ thần kinh trung ương, hoạt tính chủ vận từng phần nên có tác động giảm đau và các tác dụng khác trên thần kinh trung ương tương tự như Morphin với thời gian giảm đau thường dài hơn Morphin, có thể gây lệ thuộc thuốc nhưng tỉ lệ thấp hơn các chất chủ vận opioid như Morphin.
3. Hiệu quả lâm sàng
3.1 Chỉ định điều trị
Sixmo® được chỉ định để điều trị thay thế tình trạng lệ thuộc opioid ở những bệnh nhân trưởng thành ổn định về mặt lâm sàng, những người cần không quá 8 mg/ngày buprenorphine ngậm dưới lưỡi.
3.2 Liều lượng và cách dùng
Việc điều trị phải dưới sự giám sát của chuyên gia chăm sóc sức khỏe có kinh nghiệm trong việc quản lý tình trạng bệnh nhân lệ thuộc thuốc.
Việc đặt và rút que cấy phải được thực hiện bởi một bác sĩ có chuyên môn, mỗi đợt 4 que cấy trong thời gian sử dụng 6 tháng.
Bệnh nhân trước đây đã được điều trị bằng buprenorphine ngậm dưới lưỡi hoặc dạng phối hớp buprenorphine và naloxone ngậm dưới lưỡi, phải dùng liều ổn định từ 2 đến 8 mg/ngày trong ít nhất 30 ngày và được chuyên gia chăm sóc sức khỏe điều trị coi là ổn định về mặt lâm sàng.
3.3. Tiêu chí ngừng điều trị
Bác sĩ điều trị nên xem xét việc loại bỏ cấy ghép nếu:
• Bệnh nhân xuất hiện các dấu hiệu ngộ độc hoặc quá liều (co đồng tử, môi tím tái, an thần, nhịp tim chậm, hạ huyết áp, suy hô hấp).
• Bệnh nhân cảm thấy thiếu hiệu quả, bằng chứng là các triệu chứng cai nghiện kéo dài đòi hỏi phải điều trị lặp lại bằng buprenorphine ngậm dưới lưỡi.
3.4. Tần suất sử dụng
- Những bệnh nhân ngừng điều trị bằng Sixmo nên được chuyển trở lại liều buprenorphine ngậm dưới lưỡi trước đây của họ trong vòng 12 đến 24 giờ sau khi tháo thiết bị cấy ghép Sixmo (tức là liều mà họ đã được chuyển trước khi bắt đầu điều trị bằng Sixmo.
- Nếu muốn tiếp tục điều trị chu kỳ thứ hai, cần loại bỏ các que cấy cũ. Que cấy mới được đưa vào mặt trong của cánh tay đối diện, xác định vị trí cấy ghép thích hợp. Que cấy ghép để điều trị lặp lại nên được cấy vào dưới da càng sớm càng tốt sau khi tháo que cấy cũ trước đó, tốt nhất là trong cùng một ngày. Nếu việc cấy ghép không diễn ra trong ngày, bệnh nhân cần được duy trì liều buprenorphine ngậm dưới lưỡi cố định từ 2 đến 8 mg/ngày, theo chỉ định lâm sàng, cho đến khi điều trị lặp lại.
- Buprenorphine ngậm dưới lưỡi nên ngừng sử dụng từ 12 đến 24 giờ trước khi đặt bốn thiết bị cấy ghép Sixmo.
- Sau một lần tiêm dưới da ở mỗi cánh tay (tổng cộng là hai chu kỳ điều trị), hầu hết bệnh nhân nên được chuyển trở lại liều buprenorphine ngậm dưới lưỡi trước đây (tức là liều mà họ được chuyển sang điều trị Sixmo) để tiếp tục điều trị.
- Không có dữ liệu triển vọng nào với Sixmo sau hai chu kỳ điều trị và không có kinh nghiệm về việc cấy ghép Sixmo vào các vị trí khác của cánh tay, các vị trí khác ngoài cánh tay trên hoặc cấy ghép lại vào các vị trí đã sử dụng trước đó.
3.5. Lâm sàng trên đối tượng đặc biệt
- Người già
Các nghiên cứu lâm sàng về Sixmo không bao gồm các bệnh nhân trên 65 tuổi và do đó, việc sử dụng sản phẩm cho nhóm đối tượng này không được khuyến cáo. Hiệu quả và độ an toàn của buprenorphine ở bệnh nhân cao tuổi > 65 tuổi chưa được thiết lập.
- Suy gan
Do không thể điều chỉnh nồng độ buprenorphine trong quá trình điều trị Sixmo nên Sixmo chống chỉ định ở bệnh nhân suy gan nặng.
Bệnh nhân suy gan nhẹ đến trung bình nên được theo dõi các dấu hiệu và triệu chứng ngộ độc hoặc quá liều do tăng nồng độ buprenorphine với các triệu chứng: tím môi, lơ mơ, nhịp tim chậm, hạ huyết áp, suy hô hấp. Trong trường hợp quan sát thấy các triệu chứng ngộ độc hoặc quá liều, loại bỏ que cấy là điều bắt buộc.
- Suy thận
Sự đào thải qua thận đóng một vai trò tương đối nhỏ (khoảng 30%) trong tổng độ thanh thải của buprenorphine và nồng độ buprenorphine trong huyết tương không tăng ở bệnh nhân suy thận.
Không cần điều chỉnh liều Sixmo ở bệnh nhân suy thận. Nên thận trọng khi dùng thuốc cho bệnh nhân suy thận nặng (độ thanh thải creatinine < 30 mL/phút).
- Trẻ em
Tính an toàn và hiệu quả của Sixmo ở trẻ em dưới 18 tuổi vẫn chưa được thiết lập. Không có dữ liệu có sẵn.
4. Chống chỉ định
Bệnh nhân mẫn cảm với bất cứ thành phần nào của thuốc.
Bệnh nhân đang trong tình trạng suy giảm chức năng hô hấp mức độ nặng, suy giảm chức năng gan mức độ nặng.
Bệnh nhân bị mê sảng, bệnh nhân nghiện rượu cấp tính.
Bệnh nhân đang sử dụng thuốc ức chế men MAO hoặc trong vòng 2 tuần đã sử dụng IMAO.
Bệnh nhân là phụ nữ đang mang thai, phụ nữ đang trong thời gian nuôi con bú.
5. Tác dụng phụ
- Nhiễm trùng tại vị trí cấy que. Bệnh nhân không tự mình gỡ bỏ Probuphine .
- Nếu Probuphine rơi ra khỏi cánh tay hoặc nếu bệnh nhân ngừng điều trị, có thể có các triệu chứng run, đổ mồ hôi nhiều hơn bình thường, cảm thấy nóng hoặc lạnh hơn bình thường, chảy nước mũi, chảy nước mắt, nổi da gà, tiêu chảy, nôn mửa và đau cơ. Đó có thể là hội chứng thiếu thuốc, cần báo ngay cho bác sĩ điều trị.
- Một số tác dụng phụ thường gắp: vàng da, vàng mắt, khô miệng, táo bó, bí tiểu, phát ban, nổi mề đay, sưng mặt, thở khò khè hoặc chóng mắt, mất ý thức, tụt huyết áp tư thế.
TÀI LIỆU THAM KHẢO
- http://vidal.fr/actualites/29851-dependance-aux-opioides-sixmo-buprenorphine-en-implant-sous-cutane-de-longue-duree-d-39-action.html
- http://Titan Pharmaceuticals And Molteni Announce Positive EU CHMP Opinion For Probuphine: Titan Pharmaceuticals, Inc. (TTNP)
- Strang J, Volkow ND, Degenhardt L, et al. Opioid use disorder. Nat Rev Dis Primers. 2020;6(1):3.
- Bell J, Strang J. Medication treatment of opioid use disorder. Biol Psychiatry. 2020;87(1):82–88. doi:10.1016/j.biopsych.2019. 06.020
- Sordo L, Barrio G, Bravo MJ, et al. Mortality risk during and after opioid substitution treatment: systematic review and meta-analysis of cohort studies. BMJ. 2017;357:j1550. doi:10.1136/bmj.j1550
ThS.DS. Nguyễn Hữu Phúc
Bộ môn Hóa Dược – Hóa hữu cơ – Hóa học






